- Μαρία-Αργυρώ Καραγεώργου, Δρ. Φυσικής
- Πηνελόπη Μπουζιώτη, Διευθύντρια Ερευνών, ΕΚΕΦΕ ‘Δημόκριτος’
- Ευστάθιος Στυλιάρης, Αν. Καθηγητής, Τμήμα Φυσικής, ΕΚΠΑ
- Sanja Vranješ-Djurić, Research Professor, Vinča Institute of Nuclear Sciences, University of Belgrade
- Δημοσθένης Σταμόπουλος, Αν. Καθηγητής, Τμήμα Φυσικής, ΕΚΠΑ
Τις τελευταίες δεκαετίες η αλματώδης εξέλιξη των θετικών επιστημών και των επιστημών μηχανικού οδήγησε στην ανάπτυξη πολλών ακτινολογικών τεχνικών οι οποίες έχουν καθοριστική συνεισφορά στο στάδιο της διάγνωσης πολλών σοβαρών ασθενειών [1,2]. Οι διαγνωστικές δυνατότητες πολλών από αυτές τις τεχνικές επαυξάνονται με τη χρήση νανοδομημένων φυσικοχημικών παραγόντων οι οποίοι χορηγούνται έγκαιρα στον ασθενή συνήθως μέσω του κυκλοφορικού συστήματος [3,4].
Τα τελευταία χρόνια γίνεται έντονη έρευνα σε μια νέα κατηγορία υβριδικών ακτινολογικών παραγόντων, τους σκιαγραφικούς παράγοντες διπλής απεικονιστικής ικανότητας (dual-modality contrast agents: DMCAs), οι οποίοι μπορούν να χρησιμοποιηθούν ταυτόχρονα σε δύο θεμελιακά ανεξάρτητες ακτινολογικές τεχνικές [5]. Τα ραδιοεπισημασμένα μαγνητικά νανοσωματίδια, αποτελούν ένα τέτοιο απεικονιστικό εργαλείο, καθώς συνδυάζουν τα πλεονεκτήματα δύο διαφορετικών απεικονιστικών τεχνικών, της Υπολογιστικής Τομογραφίας Μονοφωτονικής Εκπομπής (Single Photon Emission Computed Tomography-SPECT) ή της Τομογραφίας Εκπομπής Ποζιτρονίου (Positron Emission Tomography-ΡΕΤ) με αυτή της Τομογραφίας Μαγνητικού Συντονισμού (Magnetic Resonance Imaging-MRI). Έτσι, αυτοί οι DMCAs συνδυάζουν τα πλεονεκτήματα των ανεξάρτητων απεικονιστικών τεχνικών, την υψηλή ευαισθησία των SPECT/PET με την υψηλή χωρική διακριτική ικανότητα του MRI.
Πρόσφατα, στόχος μας αποτέλεσε η ανάπτυξη δύο νανοδομημένων φυσικοχημικών DMCAs, ενός PET/MRI και ενός SPECT/MRI, και η πλήρης αξιολόγησή τους τόσο in vivo σε φυσιολογικούς και ανοσοκατεσταλμένους μύες όσο και in vitro σε περιφερικό ανθρώπινο αίμα [6-8]. Οι συγκεκριμένοι DMCAs αποτελούνται από σιδηρομαγνητικά νανοσωματίδια (ΣΝ) οξειδίων του σιδήρου (μαγνητίτης, Fe3O4), τα οποία είναι επιφανειακά επικαλυμμένα με 2,3-δικαρβοξυπροπανο-1,1-διφωσφονικό οξύ (εν συντομία, DPD) και ραδιοεπισημασμένα με τα ραδιοϊσότοπα γάλλιο-68 (68Ga) ή τεχνήτιο-99m (99mTc), αναφερόμενα ως [68Ga]Ga-DPD-Fe3O4 ή [99mTc]Tc-DPD-Fe3O4, αντίστοιχα (Εικόνα (1): αντιπροσωπευτική εικόνα Μικροσκοπίου Ατομικής Δύναμης [68Ga]Ga-DPD-Fe3O4).
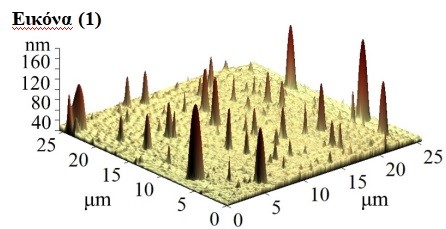
Η επιλογή των ΣΝ Fe3O4 έγινε λόγω της εγγενούς βιοσυμβατότητάς τους και της διεθνούς εμπειρίας που υπάρχει από τη χρήση τους στο MRI, τεχνική στην οποία το εξωτερικά εφαρμοζόμενο ομογενές στατικό μαγνητικό πεδίο, Hdc, μεταβάλλεται ισχυρά στην εγγύς περιοχή ενός ΣΝ, λόγω του ανομοιογενούς μαγνητικού πεδίου, HΣΝ(r), που δημιουργεί (Εικόνα (2): σχηματική απεικόνιση). Αυτό έχει ως αποτέλεσμα τη μεταβολή των χρόνων εφησυχασμού της πυρηνικής μαγνήτισης των ατόμων υδρογόνου, που βρίσκονται εντός του βεληνεκούς του HΣΝ(r).
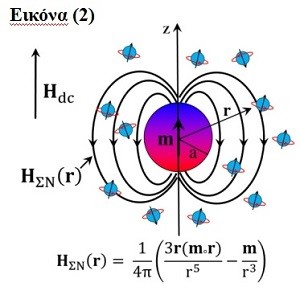
Οι μελέτες βιοκατανομών των δύο DMCAs, [68Ga]Ga-DPD-Fe3O4 και [99mTc]Tc-DPD-Fe3O4, στους μύες (Εικόνα (3): σχηματική απεικόνιση), έδειξαν ότι πρακτικά και οι δύο DMCAs προσλαμβάνονται κυρίως στο ήπαρ και στον σπλήνα (Εικόνα (4): αποτελέσματα βιοκατανομής του [68Ga]Ga-DPD-Fe3O4 σε φυσιολογικούς μύες).
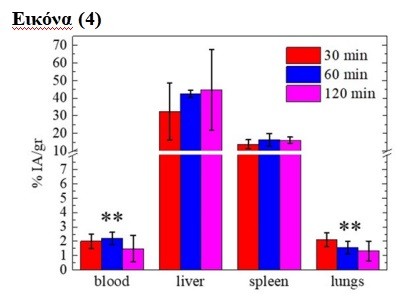
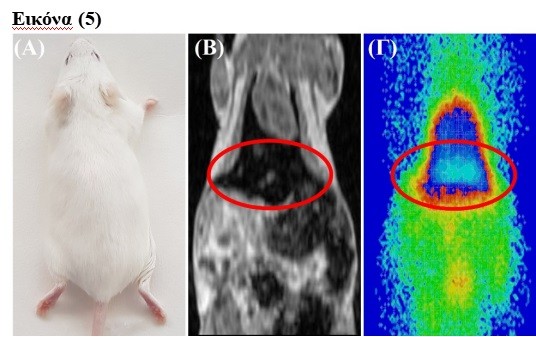
Από ανοσολογικής άποψης, η ενεργοποίηση του έμφυτου ανοσοποιητικού συστήματος, αποτελεί μια πρώτη ενθαρρυντική ένδειξη ότι οι συγκεκριμένοι DMCAs, μπορούν να αποτελέσουν ασφαλείς υποψήφιους για περαιτέρω in vivo εφαρμογές σε ανθρώπους. Η χρήση των δύο DMCAs, [68Ga]Ga-DPD-Fe3O4 και [99mTc]Tc-DPD-Fe3O4, σε συνδυαστικές απεικονίσεις PET/MRI και SPECT/MRI, έδειξε ότι η διπλή απεικονιστική ικανότητά τους είναι τουλάχιστον εφάμιλλη αυτής της ανεξάρτητης χρήσης τους (Εικόνα (5): (A) Φυσιολογικός μυς σε απεικόνιση (Β) MRI και (Γ) SPECT-Προβολική εικόνα από σύστημα γ-Camera).
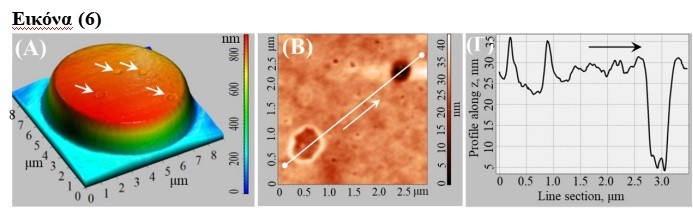
Δεδομένου ότι απώτερος στόχος της έρευνάς μας είναι οι in vivo εφαρμογές αυτών των DMCAs σε ανθρώπους, αξιολογήσαμε τη βιοσυμβατότητα του [68Ga]Ga-DPD-Fe3O4 μέσω in vitro πειραμάτων με τα έμμορφα στοιχεία περιφερικού ανθρώπινου αίματος, συγκεκριμένα με τα ερυθρά αιμοσφαίρια (Red Blood Cells-RBCs), λευκά αιμοσφαίρια (White Blood Cells-WBCs) και αιμοπετάλια (Platelets-PLTs), με χρήση συμβατικών (Optical Microscopy-OM) και προηγμένων (Atomic Force Microscopy-AFM) τεχνικών απεικόνισης [7,8]. Συνοπτικά, τα αποτελέσματα ΟΜ έδειξαν ότι τα RBCs διατήρησαν τα συνολικά μορφολογικά χαρακτηριστικά τους κατά την επώασή τους με τον DMCA [68Ga]Ga-DPD-Fe3O4. Επιπλέον, τα αποτελέσματα AFM που ελήφθησαν από την επιφάνεια των RBCs, έδειξαν μικρή αύξηση νανοσκοπικών αποδομήσεων που καταγράφονται στη μεμβράνη τους, συγκριτικά με RBCs που επωάστηκαν χωρίς τον DMCA, γεγονός που χρήζει περαιτέρω διερεύνησης (Εικόνα (6): αντιπροσωπευτικά δεδομένα AFM (Α) ενός RBC, (Β) υποπεριοχής της μεμβράνης του και (Γ) κυτταρικής τομογραφίας κατά μήκος της λευκής τομής). Όσον αφορά στα WBCs και στα PLTs, τα συνδυαστικά αποτελέσματα ΟΜ και AFM έδειξαν πως ο DMCA προώθησε την ενεργοποίησή τους, όπως αποδεικνύεται σε μικροσκοπικό και σε νανοσκοπικό επίπεδο από την αλλαγή σχήματος/μεγέθους από πλήρως σφαιρική σε πολωμένη και/ή ακανόνιστη μορφή, με την περιστασιακή εμφάνιση ψευδοποδίων στη περίπτωση των PLTs. Ωστόσο, παρά την παρατηρούμενη ενεργοποίηση τα WBCs διατήρησαν μια συμπαγή μορφή χωρίς ενδείξεις αποδόμησης, ενώ τα PLTs δεν ακολούθησαν τον καταρράκτη της πήξης.
Τα πιο πάνω συνδυαστικά in vivo και in vitro πειραματικά αποτελέσματα αποδεικνύουν πως οι συγκεκριμένοι DMCAs, [68Ga]Ga-DPD-Fe3O4 και [99mTc]Tc-DPD-Fe3O4, είναι πολλά υποσχόμενοι υποψήφιοι για μελλοντικές κλινικές δοκιμές. Επιπλέον, τόσο τα ραδιοϊσότοπα 68Ga και 99mTc, όσο και τα ΣΝ Fe3O4, ήδη χρησιμοποιούνται στην κλινική πράξη ανεξάρτητα το κάθε ένα σε διαγνωστικές και θεραπευτικές εφαρμογές. Για τον λόγο αυτό, θεωρούμε πως ο συνδυασμός τους ως DMCAs, [68Ga]Ga-DPD-Fe3O4 και [99mTc]Tc-DPD-Fe3O4, είναι επίσης ασφαλής από κλινικής άποψης έτσι που θα μπορούσαν να αξιολογηθούν σε εισαγωγικές κλινικές δοκιμές ή σε περαιτέρω in vivo πειράματα σε ανώτερα θηλαστικά.
Αναφορές
[1] Wallyn, J., Anton, N., Akram, S., and Vandamme, T.F., Biomedical Imaging: Principles, Technologies, Clinical Aspects, Contrast Agents, Limitations and Future Trends in Nanomedicines. Pharm. Res., 36, 78 (2019)
[2] Fass L., Imaging and cancer: a review. Mol Oncol., 2, 115 (2008)
[3] Arami H., Khandhar A., Liggitt D., and Krishnan K.M., In vivo delivery, pharmacokinetics, biodistribution and toxicity of iron oxide nanoparticles. Chem. Soc. Rev., 44, 8576 (2015)
[4] Wu W., Jiang C.Z., and Roy V.A.L., Designed synthesis and surface engineering strategies of magnetic iron oxide nanoparticles for biomedical applications. Nanoscale, 8, 19421 (2016)
[5] Lee N. et al. Iron oxide based nanoparticles for multimodal imaging and magnetoresponsive therapy. Chem. Rev., 115, 10637 (2015)
[6] Karageorgou M. A. et al. Gallium-68 labeled iron oxide nanoparticles coated with 2, 3-dicarboxypropane 1, 1-diphosphonic acid as potential PET/MR imaging agent: Α proof-of-concept study. Contrast Media Mol. Imaging, article ID 6951240 (2017)
[7] Karageorgou M. A., Bouziotis P., Vranjes-Djuric S. and Stamopoulos D., Hemocompatibility of gallium-68 labeled iron oxide nanoparticles coated with 2, 3-dicarboxypropane 1, 1-diphosphonic acid. Mater. Sci. Eng. C, 115, 111121 (2020)
[8] Karageorgou M. A. and Stamopoulos D., Immunocompatibility of a new dual modality contrast agent based on radiolabeled iron-oxide nanoparticles. Sci. Rep., 11, 9753 (2021)










![Συναυλία Jazz του Τμήματος Μουσικών Σπουδών ΕΚΠΑ [2 Ιουλίου]](https://hub.uoa.gr/wp-content/uploads/2025/06/Jazz-night-cover-1024x576.jpg)




